Características de Estados de Agregación
Cuando hablamos de estados de agregación o fases de la materia, nos referimos a las distintas fases o formas en que es posible encontrar la materia conocida (sustancias puras o mezclas) y que dependen del tipo y la intensidad de las fuerzas de atracción entre las partículas que componen dicha materia (tales como átomos, moléculas, etc.)
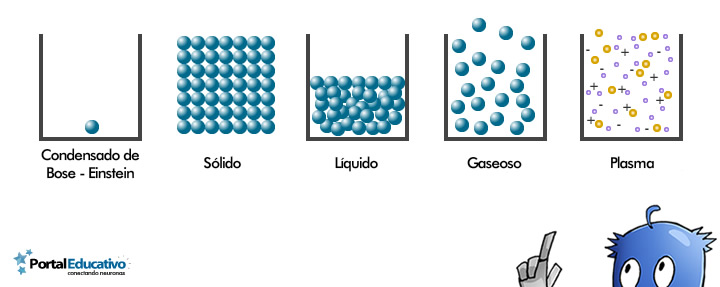
Se conocen principalmente cuatro estados de agregación de la materia: el estado sólido, el estado líquido, el estado gaseoso y el estado plasmático. También existen otros menos frecuentes, como los condensados fermiónicos, pero estas formas no se producen naturalmente en el medio ambiente..
Cada uno de los estados de agregación posee características físicas diferentes, como volumen, fluidez o resistencia, a pesar de que no exista una diferencia química real entre un estado y otro. Por ejemplo, el agua sólida (hielo) y el agua líquida (agua) son químicamente idénticas.
.
https://images.app.goo.gl/KnoBjXQutMU2M18PA
Sólido
El estado sólido se caracteriza por tener un volumen y forma definidos. En este estado, las partículas están organizadas en una estructura ordenada y compacta, lo que les otorga rigidez. Entre sus principales características se incluyen:
Las partículas vibran en posiciones fijas.
Poseen una alta densidad en comparación con los líquidos y gases.
No se adaptan a la forma del recipiente en que se encuentran.
Las fuerzas de atracción entre las partículas son fuertes, lo que impide el movimiento libre.
Existen dos tipos de sólidos: cristales, que tienen un orden interno regular, y amorfo, que son desordenados en su estructura.
Ejemplos de sólidos incluyen metales, minerales y hielo.
Líquido
El estado líquido es uno de los estados más versátiles de la materia. En este estado, las partículas tienen más libertad de movimiento en comparación con los sólidos, lo que les permite fluir y adaptarse a la forma de su recipiente. Algunas características del estado líquido son:
El líquido tiene un volumen definido, pero no una forma fija.
Las partículas están más separadas que en los sólidos, permitiendo que fluyan.
Se puede comprimir solo mínimamente; sin embargo, es menos denso que los sólidos.
Ejemplos comunes de líquidos incluyen agua, aceites y soluciones.. Su comportamiento es esencial en diversos procesos físicos y químicos.
Gaseoso
El estado gaseoso se caracteriza por la ausencia de forma y volumen definidos. Las partículas en este estado tienen una gran cantidad de energía y se encuentran en constante movimiento. Algunas de sus principales propiedades son:
Las partículas están muy separadas y se mueven libremente en todas direcciones.
El gas expandirá para llenar cualquier recipiente, adaptándose a su forma.
Son compresibles, lo que significa que su volumen se puede reducir aplicando presión.
Ejemplos de gases incluyen el aire, el oxígeno y el dióxido de carbono.
El estudio del comportamiento de los gases es crucial en diversas aplicaciones científicas y tecnológicas.
Plasma
El estado plasmático es considerado el cuarto estado de la materia. Se forma a partir de gases ionizados, es decir, cuando las partículas de un gas se ionizan, creando un conjunto de electrones libres y iones positivos. Este estado es común en el universo, siendo el componente principal de estrellas, incluidos nuestro sol. Algunas propiedades del plasma son:
Conductor de electricidad, debido a la presencia de partículas cargadas.
Se puede influenciar mediante campos eléctricos y magnéticos.
Su temperatura puede ser extremadamente alta, lo que provoca una fuerte emisión de luz.
Ejemplos de plasmas incluyen auroras boreales, rayos y la materia en el interior de las estrellas.
https://s1.significados.com/foto/cambios-de-estado-de-la-materia-f1_bg.jpg?class=article
Puede obligarse a la materia a pasar de un estado de agregación a otro, tan solo alterando la temperatura y la presión en las que se encuentra. Así, se puede hervir agua líquida para llevarla al estado gaseoso (vapor) o se puede enfriar lo suficiente como para llevarla al estado sólido (hielo).
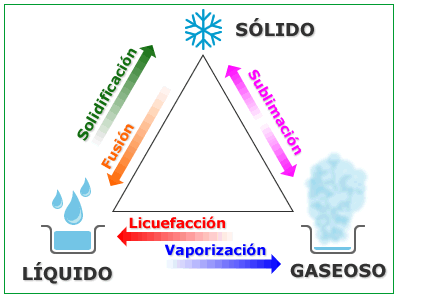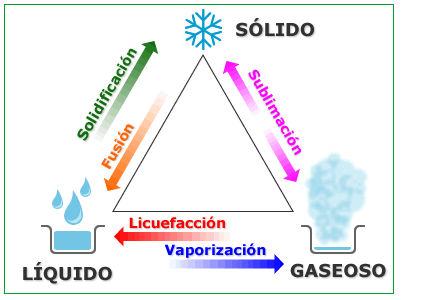
Estos procedimientos de transformación de un estado de agregación de la materia a otro suelen ser reversibles, aunque no sin cierto margen de pérdida de la sustancia. Los procesos más conocidos son los siguientes:
Fusión. Es el proceso mediante el cual al suministrar energía calórica (calor), un sólido puede transformarse en líquido.
Solidificación: Es el proceso mediante el cual al aumentar la presión, un líquido puede transformarse en sólido.
Evaporación. Es el proceso mediante el cual al introducir energía calórica (calor), parte de la masa de un líquido (no necesariamente la totalidad de la masa) se transforma en gas.
Ebullición o vaporización. Es el proceso mediante el cual al suministrar energía calórica, la totalidad de masa de un líquido se transforma en un gas. La transición de fase ocurre cuando la temperatura supera el punto de ebullición del líquido (temperatura a la cual la presión del vapor del líquido se iguala a la presión que rodea al líquido, por tanto, se convierte en vapor).
Condensación :Es el proceso mediante el cual al retirar energía calórica, un gas se transforma en un líquido. Este proceso es contrario a la vaporización.
Licuefacción. Es el proceso mediante el cual al aumentar mucho la presión, un gas se transforma en un líquido. En este proceso, el gas también se somete a bajas temperaturas, pero lo que lo caracteriza es la elevada presión a la que es sometido el gas.
Sublimación. Es el proceso mediante el cual al suministrar calor, un sólido se transforma en gas, sin pasar antes por el estado líquido.
Deposición o sublimación inversa. Es el proceso mediante el cual al retirar calor, un gas se transforma en sólido, sin pasar antes por el estado líquido.
Ionización: Cambio de Gas a plasma.
Deionización: Cambio de Plasma a gas estos se realizan en condiciones controladas en laboratorios especializados
Los conocimientos sobre los estados de agregación de la materia tienen numerosas aplicaciones en la vida cotidiana. En la industria alimentaria, se utilizan procesos de congelación, ebullición y destilación para preservar y transformar alimentos. En la farmacéutica, el conocimiento sobre las propiedades de los distintos estados de materia es crucial para el desarrollo de medicamentos.
En la tecnología, se desarrollan materiales a partir de distintos estados de la materia, como plásticos, metales y cerámicas. Además, en la meteorología, el estudio de los cambios de estado del agua permite comprender fenómenos como la lluvia, nieve y vapor. Así, la comprensión de cuales son los estados de agregación de la materia es fundamental en múltiples disciplinas.