Concepto

La composición centesimal
Este indica el porcentaje en masa, de cada elemento que forma parte de un compuesto.Se obtiene por análisis gravimétrico y conociendo los pesos atómicos de los compuestos puede determinarse su fórmula mínima o molecular.
La palabra composición (del latín “compositio” se refiere a la acción y al efecto de componer, verbo, cuyo nombre se deriva del latín “componere”, vocablo integrado por el prefijo “con” que indica “reunión” y por “ponere” que se traduce como “poner”, por lo cual una composición es una reunión de elementos puestos en orden, con un objetivo, por lo cual se usa en varios ámbitos.
En Química, una composición, hace referencia a cómo, con qué elementos y en qué proporción se forma un compuesto, lo que se expresa en fórmulas, por ejemplo, cuando compramos un medicamento podemos leer en su prospecto los distintos elementos y la cantidad de ellos, que intervienen en su elaboración.
La Composición Centesimal (CC) es una medida de la cantidad de masa que ocupa un elemento en un compuesto. Se mide en porcentaje de masa
La Composición Centesimal es útil para obtener la fórmula empírica y molecular de un compuesto
La composición cuantitativa de las sustancias y reacciones químicas entre las mismas.
El mol Es la unidad de cantidad y conteo de sustancias, que se determina en función a la cuantía de las mismas que contiene el mismo número de unidades.
Los compuestos se representan mediante fórmulas químicas, que expresan la composición cualitativa y cuantitativa que tiene una sustancia dada. Es decir, la fórmula contiene los símbolos de los elementos que forman la sustancia y unos números en forma de subíndices que indican el número de átomos en lo que se denomina entidad elemental.
Es la masa atómica en gramos de un elemento que contiene el número Avogadro de átomos y que se mide, cambiando las unidades de la masa atómica del elemento de Uma a gramos.
La masa molar de los compuestos, se calcula sumando las masas molares de cada uno de los átomos presentes en la formula.
Cada año se sintetizan o se descubren en la naturaleza miles de compuestos nuevos. Unos de los primeros pasos para sintetizar un compuesto nuevo es determinar su composición porcentual, para lo cual se realiza un análisis cualitativo que determina los elementos presentes en un compuesto. La composición porcentual o centesimal indica el porcentaje en masa, de cada elemento que forma parte de un compuesto. Básicamente se puede definir como: una parte dividida entre todas las partes multiplicada por 100. Se obtiene por análisis gravimétrico y conociendo los pesos atómicos de los compuestos puede determinarse su fórmula empírica o molecular. También se obtiene a partir de la fórmula molecular del compuesto, ya que ésta nos indica el número de átomos de cada elemento presentes en el compuesto. Forma parte de los cálculos estequiométricos, y fue de gran importancia en la Historia de la química para la determinación de los pesos atómicos y moleculares, por ejemplo, en los trabajos de Berzelius y Cannizzaro en los antecedentes de la Tabla Periódica de los Elementos químicos
La composición centesimal del amoniaco es por lo tanto: 82,35% de nitrógeno y 17,65% de hidrógeno.
El amoniaco es un compuesto químico cuya molécula está formada por un átomo de nitrógeno (N) y tres átomos de hidrógeno (H) de acuerdo a la fórmula NH3. La molécula no es plana, sino que presenta una forma tetraédrica con un vértice vacante, y ello es debido a la formación de orbitales híbridos sp³.
La composición centesimal indica el porcentaje, en masa, de cada elemento que forma parte de un compuesto. Se obtiene a partir de la fórmula molecular del compuesto, ya que ésta nos indica el número de átomos de cada elemento presentes en el compuesto.
Cómo calcular la composición
Se divide la contribución de cada elemento entre la masa molecular o masa de fórmula y ese resultado se multiplica por 100. Ese es el porcentaje de cada uno de los elementos constituyentes del compuesto. La suma de los porcentajes de todos los elementos constituyentes es igual a 100.
En el caso del agua su molécula es H2O. Supongamos que tenemos que calcular el % de hidrógeno y de oxígeno que hay en el agua. Obviamente no importa que masa de agua tengamos. Podrían ser 200 g, 600 g o 5 kg. Los porcentajes no varían.
Primero debemos calcular el peso molecular del agua.
En la tabla periódica tenemos todos estos datos a mano.
El oxígeno pesa 16 y el hidrógeno 1. Así que la molécula de agua tiene un peso total relativo de 18 que expresado como mol (peso molecular en gramos) nos dará 18 g
Con una regla de tres simple calculamos perfectamente los porcentajes.
Para el oxígeno:
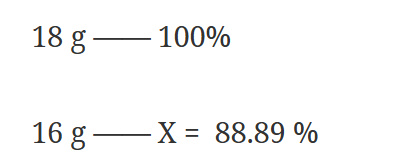
El 100 % esta representado por la masa total de la molécula que es de 18 g. El cálculo lo hacemos como producto cruzado y división derecha como toda regla de tres. 16 x 100 / 18 = 88,89 %.
Para el hidrógeno:
18 g —— 100%
2 g —— X = 11,11 %
También este último porcentaje lo podemos obtener restando al 100 % el 88,89 % del oxígeno. La suma de ambos porcentajes nos debe dar siempre 100 %.
Segundo Procedimiento
Ejemplo :: Calcular la composición centesimal del H y O en el agua si en 45 gramos de agua hay 5 de H y 40 de O:
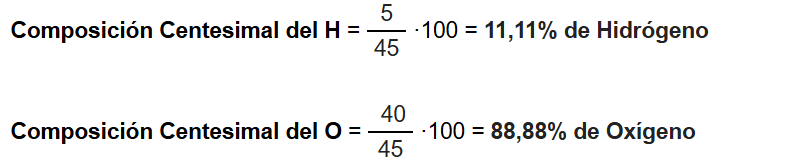
En el caso anterior calcular la Fórmula Empírica del agua sabiendo que las masas atómicas del H y O son respectivamente 1 y 16:
Para calcuar la fórmula empírica se divide la composición centesimal entre la masa atómica del elemento. Acto seguido se dividen los resultados por el valor más pequeño de ambos:
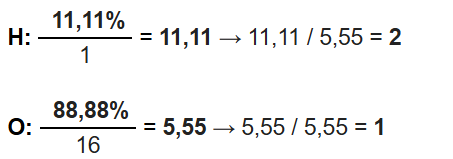
Por lo tanto la fórmula empírica del agua es: H2O
Ejercicio 2: Una muestra de hidrocarburo de 85 gramos contiene unas cantidades de Carbono e Hidrógeno de 68 y 17 gramos respectivamente. Calcular sus composiciones centesimales:
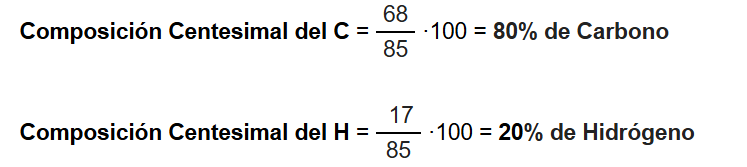
Parte II.- Calcular las fórmulas empírica y molecular del hidrocarburo del ejercicio anterior si su peso molecular es 30g/mol:
Para calcuar la fórmula empírica se divide la composición centesimal entre la masa atómica del elemento. Acto seguido se dividen los resultados por el valor más pequeño de ambos:
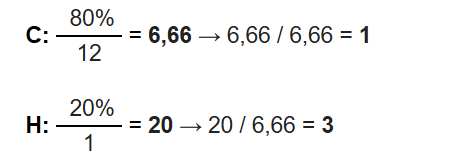
Por lo tanto la fórmula empírica del hidrocarburo es: CH3
Para calcular la fórmula molecular se calcula cuántas veces necesitamos multiplicar la fórmula empírica para alcanzar el peso molecular (30g/mol):
n ·Peso molecular (CH3) = 30 → n · 15 = 30 → n = 2
Por lo tanto, la fórmula molecular del hidrocarburo es: C2H6 es decir, se trata del etano (CH3-CH3)