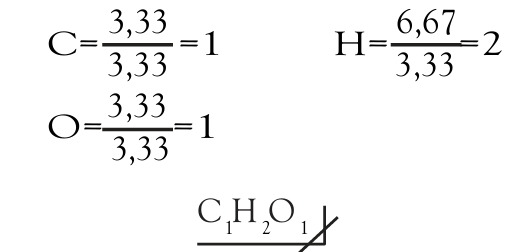LA COMPOSICIÓN PORCENTUAL ES :
La fórmula de un compuesto, indica la cantidad de átomos de cada elemento en una unidad del compuesto. Imaginemos la siguiente situación, se compra a una distribuidora de insumos químicos una cantidad de un ácido para realizar una actividad demostrativa, y al observar el etiquetado se quiere verificar su pureza. A partir de la fórmula es posible calcular el porcentaje de cada elemento. De esta manera se puede comparar con el porcentaje obtenido experimentalmente de la muestra, es posible calcular su grado de pureza
.
LA COMPOSICIÓN PORCENTUAL ES EL PORCENTAJE EN MASA DE CADA ELEMENTO EN UN COMPUESTO.
Para obtener el porcentaje de cada elemento primero se debe conocer la masa molar del compuesto, ya que representa el 100% de la masa.
Etanol o también llamado alcohol Etílico, cuya fórmula química corresponde a C2H6O.
Calcule la composición porcentual del Etanol, si se sabe que las masas molares de los elementos constituyentes son: C=12 ;g/mol, H= 1 g/mol, y O= 16 g/mol
Procedimiento
C2H6O
Masa molar (MM)= ( (2x 12g/mol) + (6x 1g/mol) + 16 g/mol)= 46 g/mol
Cálculo de porcentaje de Carbono en el compuesto.
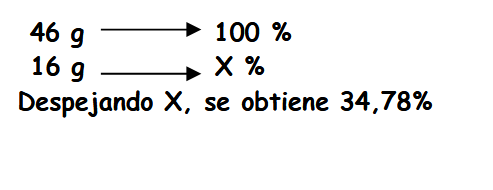
Si 46 gramos equivalen al 100 %, y hay 24 gramos de Carbono, entones se plantea la siguiente proporción:


Ejemplo : Halla la composición centesimal de los átomos en los compuestos.

Halla la composición centesimal de los siguientes compuestos:
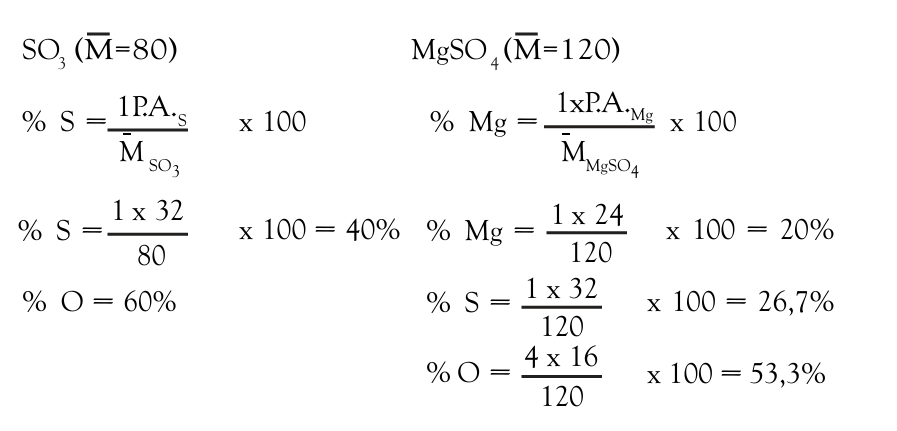
Se encontró un compuesto constituido por C, O y H donde se tiene 40% de C, 6,67% de H y 53,33% de O. Determina su fórmula empírica.
Resolución:
C = 40% H = 6,67% O= 53,33%
1.er paso:
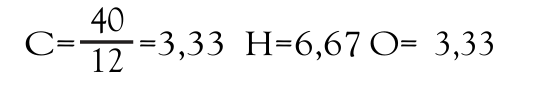
2.° paso: Dividimos entre el menor