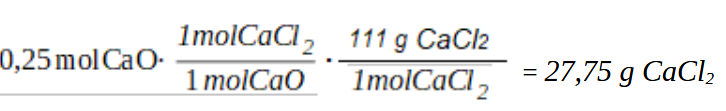En una reacción química siempre se conserva la masa, de ahí que una cantidad específica de reactivos al reaccionar, formará productos cuya masa será igual a la de los
reactivos. Al químico le interesa entonces la relación que guardan entre sí las masas de los reactivos y los productos individualmente
Las distintas operaciones matemáticas que permiten calculara la cantidad de una sustancia que reacciona o se produce en una determinada reacción química.
Una reacción se produce en condiciones estequiométricas cuando las cantidades de reactivos en las proporciones idénticas a las de la ecuación química ajustada
Los datos sobre los reactivos y los productos no se expresan, normalmente, en cantidad de sustancias ( moles ), sino que se expresan en masa ( gramos ) o en volumen ( litros) de disolución o de gas
Dando lugar a procedimientos General en los cálculos estequiométricos
Escribe la ecuación química ajustada
Calcula los moles de sustancias datos
Usa la relación estequiométrica para obtener los moles de la sustancias incógnita
Convierte los moles de la sustancia incógnita a la magnitud pedida
Los cálculos que comprenden estas relaciones de masa se conocen como cálculos estequiométricos.
La estequiometría es el concepto usado para designar a la parte de la química que estudia las relaciones cuantitativas de las sustancias y sus reacciones. En su origen
etimológico, se compone de dos raíces , estequio que se refiere a las partes o elementos de los compuestos y metría, que dice sobre la medida de las masas.
Cuando se expresa una reacción, la primera condición para los cálculos estequiométricos es que se encuentre balanceada, por ejemplo :
Mg + O2 → MgO
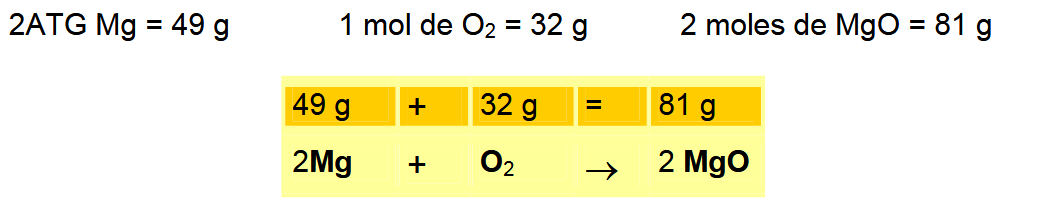
2 Mg + O2 → 2 MgO Reacción balanceada
La reacción anterior se lee como : 2 ATG de Magnesio reaccionan con un mol de Oxígeno y producen 2 moles de Óxido de magnesio
Como calcular los ATG de un elemento en un X cantidad de elemento
Por ejemplo :¿Cuántos ATG se encuentran contenidos en 54 g de Al?
1.- Consultar la tabla periódica el peso atómico del Aluminio
2.- Relacionar mediante un regla de tres
1 ATG de Al ---- 27 g
X ---- 54 g
Despegar la X = 1 ATG de Al ( 54 g ) / 27 g = = 2 ATG
¿4.5 ATG de Pb a cuántos g equivalen ?
1 ATG de Pb ---- 207 g
4.5 ATG ----. X X = (4.5 ATG) (207 g ) / 1 ATG de Pb = 931.5 g
MOLES
¿Cuántos moles se encuentran contenidos en 120 g de H2O?
1 mol de H2O ---- 18 g
X ---- 120 g X = (1 mol H2O ) (120 g H2O ) / 18 g X = 6.6 moles
¿ 0.6 moles, de NaNO2 a cuántos g equivalen ?
1 mol de NaNO2 ---- 69 g
0.6 moles ---- X X = (0.6 moles ) (69 g ) / 1 mol e NaNO2 X = 41.4 g
No. DE ATOMOS Y No. DE MOLÉCULAS
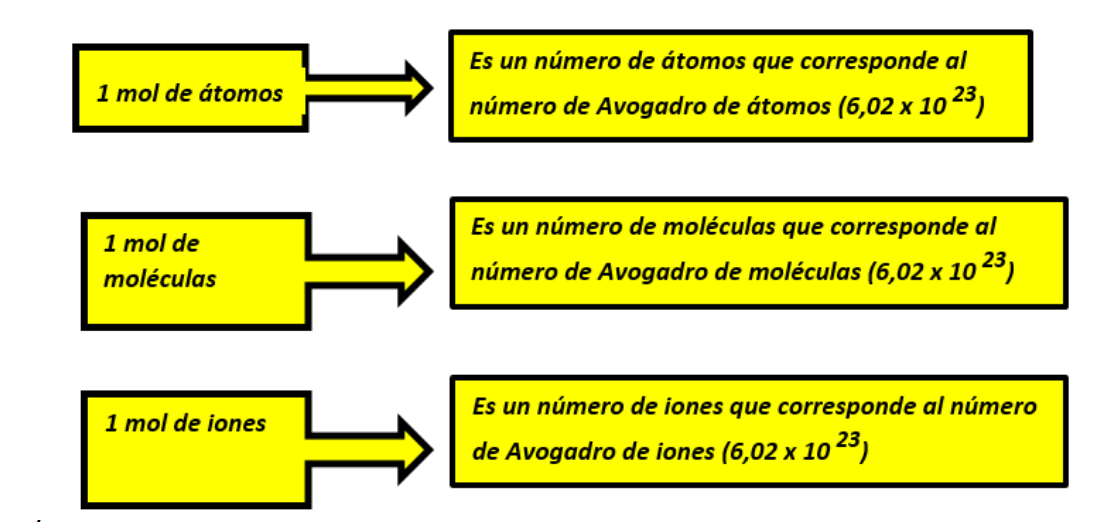
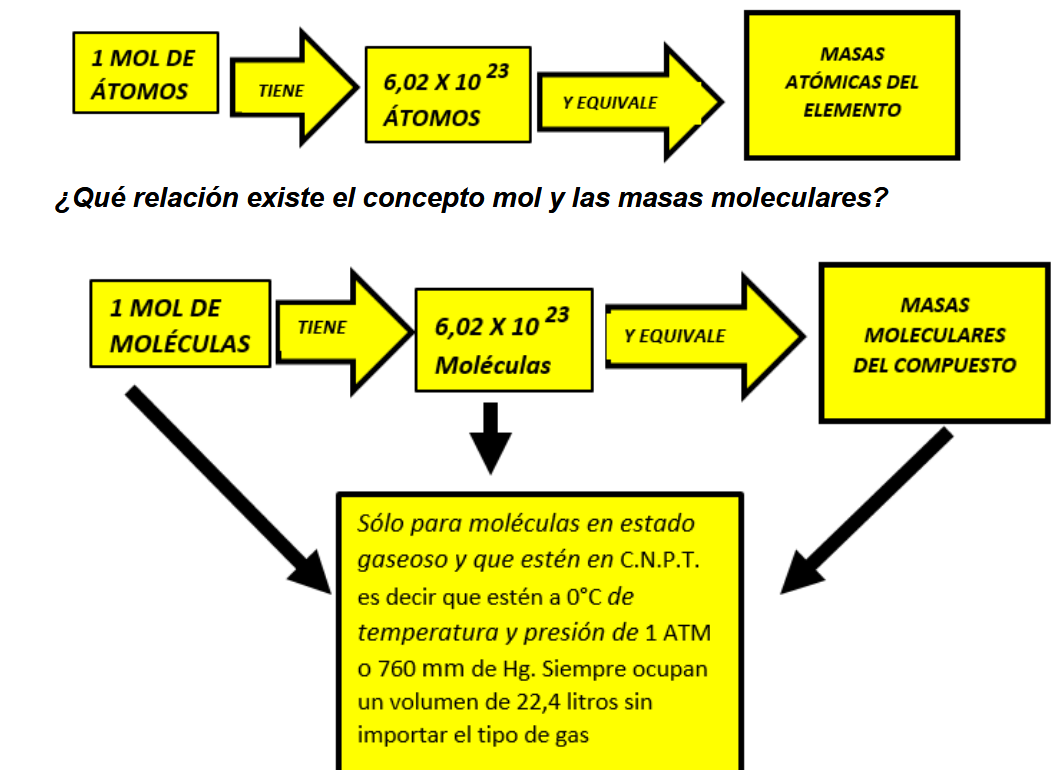
1 ATG de cualquier elemento contiene 6.023 X 10 23 átomos y 1 mol de cualquier compuesto tiene 6.023 X 10 23 moléculas.
El número 6.023 X 10 23 es conocido como número de Avogadro (N) .
1 ATG de Cu ---- 6.023 X 10 23 átomos
15 ATG -- ---------- X X = (15 ATG ) (6.023 X 10 23) / 1 XATG de Cu = 9.023 X 10 24 átomos
¿ Cuántos átomos están contenidos en 230 g de Níquel ?
Convertir g a ATG (230g = 3.93 ATG)
1 ATG de Ni ---- 6.023 X 10 23 átomos
3.93 ATG -.-------------- X X = (3.93ATG ) (6.023 X 10 23 átomos ) / 1 ATG de Ni = 2.36 X 10 24 átomos
¿Cuántas moléculas están contenidas en 0.25 moles de CO2 ?
1 mol de CO2 ---- 6.023 X 10 23 moléculas
0.25 moles --- ---------- X X = (0.25 moles ) (6.023 X 10 23 ) / 1 X = 1.5 X 10 23 moléculas
¿Cuántas moléculas están contenidas en 10 g de HCl ?
Convertir g a moles (10g = 0.27 moles)
1 mol de HCl ---- 6.023 X 10 23 moléculas
0.27 moles --------------- X X = (0.27moles ) (6.023 X 10 23) / 1 mol de HCl X = 1.6 X 10 23 moléculas
Calculo Mol- Mol
Para dar cumplimiento a la ley de la conservación de la materia, el cálculo se efectúa en una ecuación química balanceada.
Si se conoce la cantidad de moléculas (moles) que intervienen en una reacción química, se puede establecer el número de moles de un reactivo o
producto de interés.
Procedimiento
La preparación de dicloruro de calcio tiene lugar según: CaO + HCl = CaCl2 + H2O
a) Ajusta la reacción química.
b) Calcula los moles de CaCl2 que se obtendrán a partir de 0,25 moles de CaO.
Datos: M(Ca) = 40; M(O) = 16; M(H) = 1; M(Cl) = 35,5)
Ajuste de reacción CaO + 2 HCl = CaCl2 + H2O
b) .- Ahora partimos de moles de datos (0,25 mol CaO) y, por factor de conversión (utilizando los coeficientes estequiométricos y vemos que 1 mol de CaO produce 1 mol de CaCl2. Así convertimos de moles de datos a moles de incógnita, que es lo que nos piden.
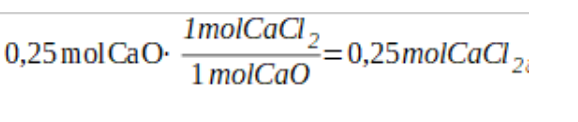
Cálculos mol-gramo
Toma los datos del ejemplo anterior y calcula los gramos de CaCl2 que se obtendrán con 0,25 moles de CaO
0.25 mol CaCl2 = 1 mol CaCl2 ( 111 g CaCl2 ) =27.75 g
1.- Hemos pasado de mol de dato a mol de incógnita (utilizamos los coeficientes estequiométricos y según la ecuación, 1 mol de CaO produce 1 mol de CaCl2).
2.- Hemos pasado de mol de incógnita a gramos de incógnita (utilizando su peso molecular). Para CaCl2 su peso molecular son 111 g/mol y por lo tanto, 1 mol de CaCl2 equivalen a 111g de CaCl2 . (Ca = 40 y Cl =35,5, por lo que Pm = 40 + 2*35,5 =111 g/mol )