Antecedentes Históricos
• Teoría de los cuatro elementos (Empédocles)
• Teoría atomística (Leucipo y Demócrito)
• Teoría de materia continua (Aristóteles)
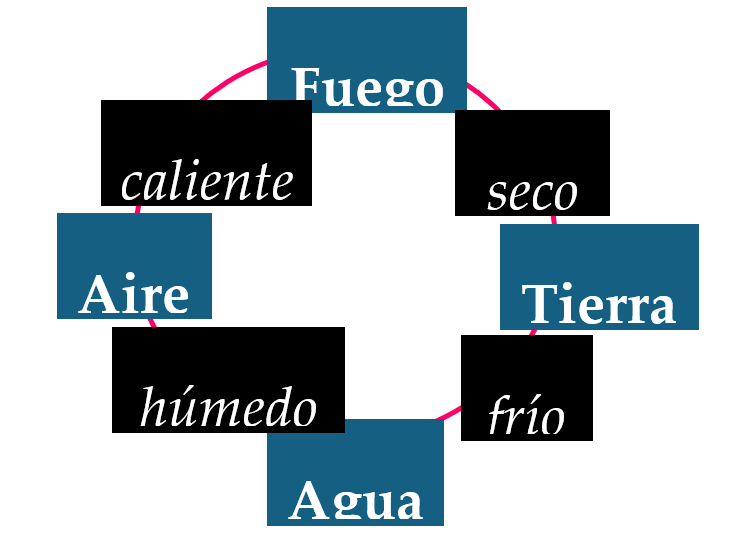
• Alquimia: Azufre, mercurio y sal
Piedra filosofal
Elixir de la vida.
• Siglo XVIII: análisis gravimétrico cuantitativo
Leyes de la química.
Sustancias químicas (clasificación)
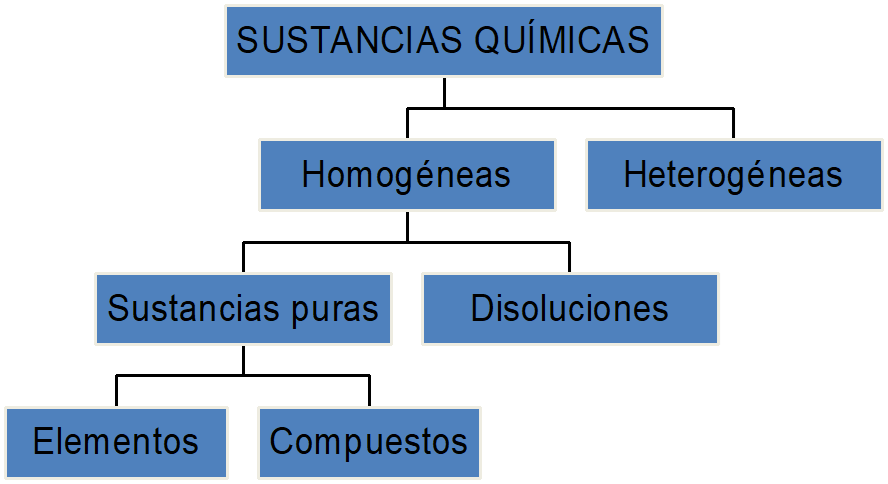
Leyes fundamentales de la Química.
• Ley de conservación de la masa (Lavoisier).
• Ley de proporciones definidas (Proust).
• Ley de proporciones múltiples (Dalton).
• Ley de proporciones recíprocas (Ritcher)
• Ley de volúmenes de combinación (Gay-Lussac).
![]()
TEORÍA ATÓMICA DE DALTON
 Hipótesis de Avogadro
Hipótesis de Avogadro
Cuando se desea determinar la forma en que se combinan dos elementos a través de una reacción química, deben tomarse en cuenta las cuatro leyes que se describen a continuación.
Ley de conservación de la masa (Lavoisier).
“En toda transformación química la masa se conserva, es decir, la masa total de los reactivos es igual a la masa total de los productos de la reacción”.
La ley de Lavoisier se aplica a cada instante porque permite representar una reacción química por una igualdad llamada ecuación química. Los cálculos basados en las ecuaciones químicas son los más importantes de la química general, y en cuanto a las unidades de peso, podemos expresar en gramos, kilogramos, toneladas u otras, unidades de peso como ser libras,
Ejemplo:
Si reaccionan 12 g. de carbono con 32 g de oxígeno dan 44 g. de CO2
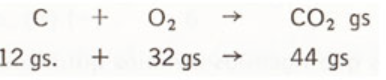
2 gramos de cloro y 3 gramos de sodio producen 5 gramos de cloruro de sodio.
2 g Cl + 3 g Na = 5 g NaCl
Esta ley ha sido probada experimentalmente con la balanza de precisión, pesando la materia antes y después de la reacción, y así formuló su ley en 1.789.
La consecuencia lógica de esta ley es que la materia no se puede crear ni destruir: sólo se puede transformar, ya que en las reacciones químicas una clase de materia se transforma en otra. Sin aumentar ni disminuir su peso total.
Sin embargo, se ha demostrado modernamente que la materia puede destruirse como tal, transformándose en energía es decir en calor, luz, etc., de todos modos, la destrucción de la materia en las reacciones químicas es infinitamente pequeña, por lo que es despreciable (teoría de la relatividad).
Por esto la ley de la conservación de la materia tiene su validez.
Ley de proporciones definidas (Proust).
• “Los elementos se combinan para formar compuestos en una proporción de masa fija y definida”.
Se llama también ley de las proporciones definidas o constantes, fue formulada en el año 1.806 y dice:
“Cuando dos o más cuerpos se combinan para formar un compuesto determinado, siempre lo hacen en proporciones fijas definidas e invariables. Fuera de Estas proporciones el excedente no interviene en la reacción”.
Esto quiere decir, que un compuesto siempre tiene la misma composición, sin que interese su procedencia ni el método con que se obtenga.
Así por ejemplo el H Cl obtenido por cualquier método, ya sea por síntesis o por la acción del H2 SO4 sobre Na Cl, se forma siempre en la proporción de 35,5 gs. de cloro por 1 gramo de hidrógeno.
El agua resulta de la unión de dos gramos de hidrógeno con 8 gramos de oxígeno, si hay exceso de uno o de otro elemento la parte que sobra no entra en la combinación, queda libre si se efectúa el análisis del agua dará también las mismas proporciones indicadas.
Esta ley permite distinguir un compuesto químico de una mezcla, puesto que en la mezcla de sustancias los constituyentes pueden tener cualquier proporción, en cambio en las combinaciones químicas lo hacen en cantidades fijas e invariables.
Los elementos de un compuesto entran en un determinado porcentaje, con el porcentaje de estos elementos se puede determinar la fórmula empírica y molecular, tal como se hizo en las lecciones anteriores.
Como quiera que en química se trabajan en cantidades pequeñas, se puede expresar utilizando cantidades menores como ser: mitades, décimos, milésimos, etc., (sub-múltiplos).
Ejemplo: El azufre y el hierro se combinan para formar sulfuro de hierro (II) en la siguiente proporción: 4 gramos de azufre por cada 7 gramos de hierro.
12 g de C + 32 g de O = 44 g de CO2
6 g de C + 16 g de O = 22 g de CO2
3 g de C + 8 g de O = 11 g de CO2
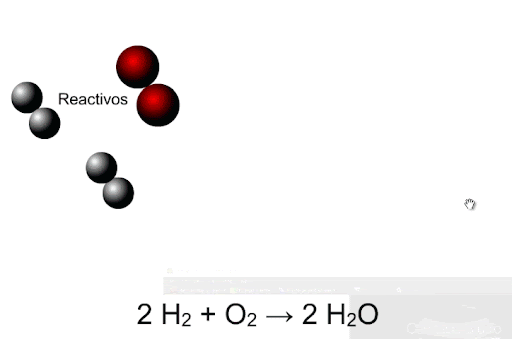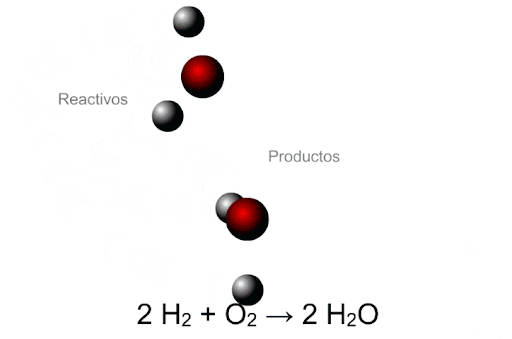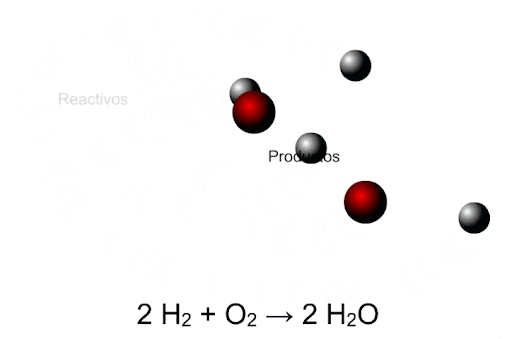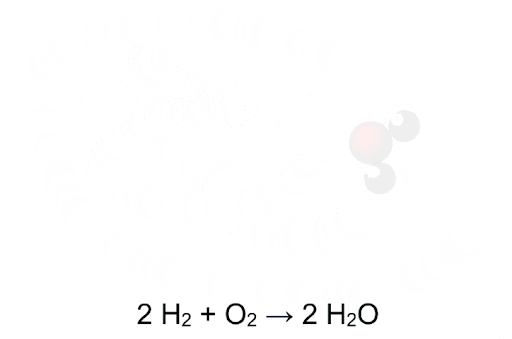
Ley de las proporciones múltiples
Ley de Dalton (Químico inglés). Se llama también ley de las proporciones múltiples y fue formulada el año 1.803 y dice:
“Cuando dos elementos se combinan para formar varios compuestos s e que el peso de uno de ellos permanece constante, mientras que el peso del otro varía en proporciones" múltiples del peso mínimo de dicho elemento”.
Según esta ley, si se da una combinación entre dos elementos para generar más de un compuesto, entonces la masa de uno de los elementos se une con una masa invariable del otro, conservando una relación que se manifiesta a través de números enteros pequeños.
Se dan como ejemplo el dióxido y el monóxido de carbono, que son dos sustancias constituidas por los mismos elementos, pero en el dióxido se relacionan como O/C=2:1 (por cada átomo de C hay dos de O) y en el monóxido su relación es 1:1.
Así por ejemplo el nitrógeno con el oxígeno forma varios compuestos combinándose en un principio un mismo peso de N2 con diferentes pesos de oxígeno para dar:

Obsérvese que los elementos horizontales expresan la ley de Proust o de las proporciones definidas.
Se llama ley de Dalton porque, aunque él no la descubrió, su teoría sirvió para explicarla.
Ley de las proporciones recíprocas (o “Ley de las proporciones equivalentes”)
Ley de Richter. Químico alemán, se llama también de las proporciones recíprocas o de los pesos equivalentes, fue formulada en 1762 y comprobada en 1.807 y dice:
“Los pesos de dos elementos que reaccionan con el mismo peso de un tercer elemento, sorprendentemente también pueden reaccionar entre sí en la misma proporción o en sus múltiplos”.
Esta ley permitió establecer el peso de combinación o peso equivalente gramo de un elemento, que es el número de gramos del mismo que se combinarán con, o desplazarán 8 g. de oxígeno o 1,008 g. de hidrógeno, así el peso equivalente gramo (p, eq, g) del calcio es 20 g. porque es la cantidad que se combina con 8 g. de oxígeno.
Ejemplo. En los compuestos oxigenados del azufre se puede demostrar la ley de Richter tomando como patrón el (p, eq, g) del oxígeno.

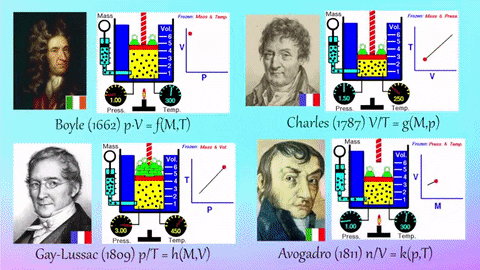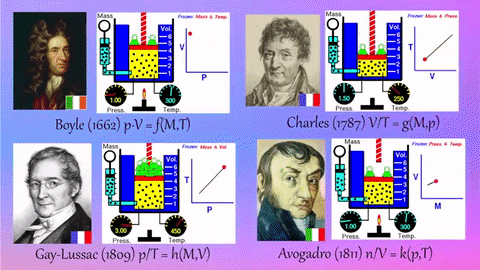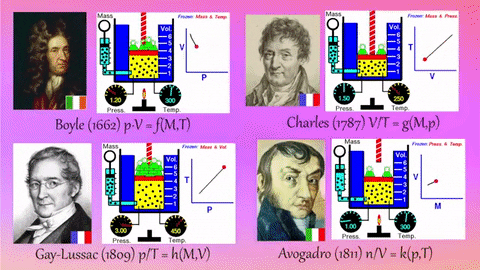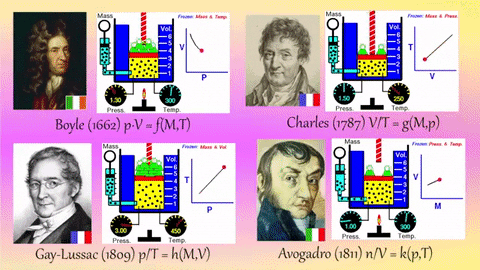
Ley de volúmenes de combinación (Gay-Lussac).
• 1 litro de oxígeno se combina con 2 litros de hidrógeno para dar 2 litros de agua (gas).
1 litro de hidrógeno se combina con 1 litro de cloro para dar 2 litros de cloruro de hidrógeno.
•1 litro de nitrógeno se combina con 3 litros de hidrógeno para dar 2 litros de amoniaco.
https://tse2.mm.bing.net/th?id=OIP.7-29egnmy8bWZIq2J9L-GQHaEK&pid=Api&P=0&h=180