https://images.app.goo.gl/CYbqRA25W5Yzgkb29
Nuestro paradigma actual acerca de la estructura de la materia es que ésta es discontinua, es decir que está constituida por pequeños corpúsculos separados por espacio vacío.
Esta idea acerca de la materia no ha sido siempre así. Durante siglos fue exactamente opuesta. Aristóteles (siglo IV a C), filósofo griego cuyas ideas influyeron durante siglos en las concepciones científicas de nuestra civilización, pensaba que el espacio vacío no podía existir en la naturaleza; con lo cual la composición de la materia debía ser continua.
En la actualidad se utiliza la Teoría cinético-corpuscular para dar un marco conceptual a la estructura de la materia discontinua. Esta teoría tiene tres postulados (aunque este número depende de la manera de enunciarla):
1. La materia está formada por pequeños corpúsculos en constante movimiento, separados por espacio vacío. Como ya sabemos estos pequeños corpúsculos pueden ser átomos, iones o moléculas; dependiendo del tipo de sustancia considerada.
2. Los corpúsculos que forman a la materia ejercen entre sí fuerzas de atracción o cohesión de diferente intensidad. La intensidad de estas fuerzas depende del tipo de corpúsculo, de la distancia a la cual se encuentren y de la velocidad a la cual se mueven estos corpúsculos.
3. La temperatura de un cuerpo es proporcional a la velocidad promedio de los corpúsculos que lo forman. Cuanto mayor sea la velocidad promedio de los corpúsculos, mayor será la temperatura del cuerpo.
El modelo cinético resultó tan eficaz para explicar el comportamiento de los gases que posteriormente, y gracias a los trabajos de los físicos L. E. Boltzmann y J. C. Maxwell, se extendió a los otros dos estados: líquido y sólido. permite explicar las propiedades de los tres estados de agregación de la materia: sólido, líquido y gaseoso.
Además, esta teoría plantea que entre las partículas que constituyen la materia existen unas fuerzas de atracción que son tanto más intensas cuanto más cerca se encuentren las partículas entre sí.
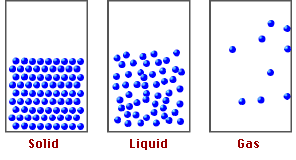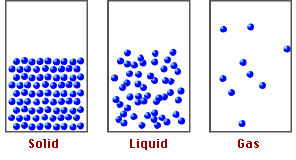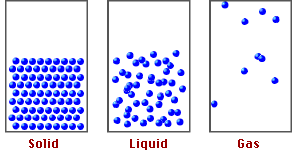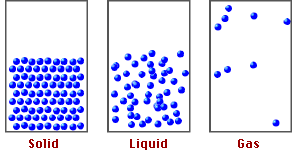
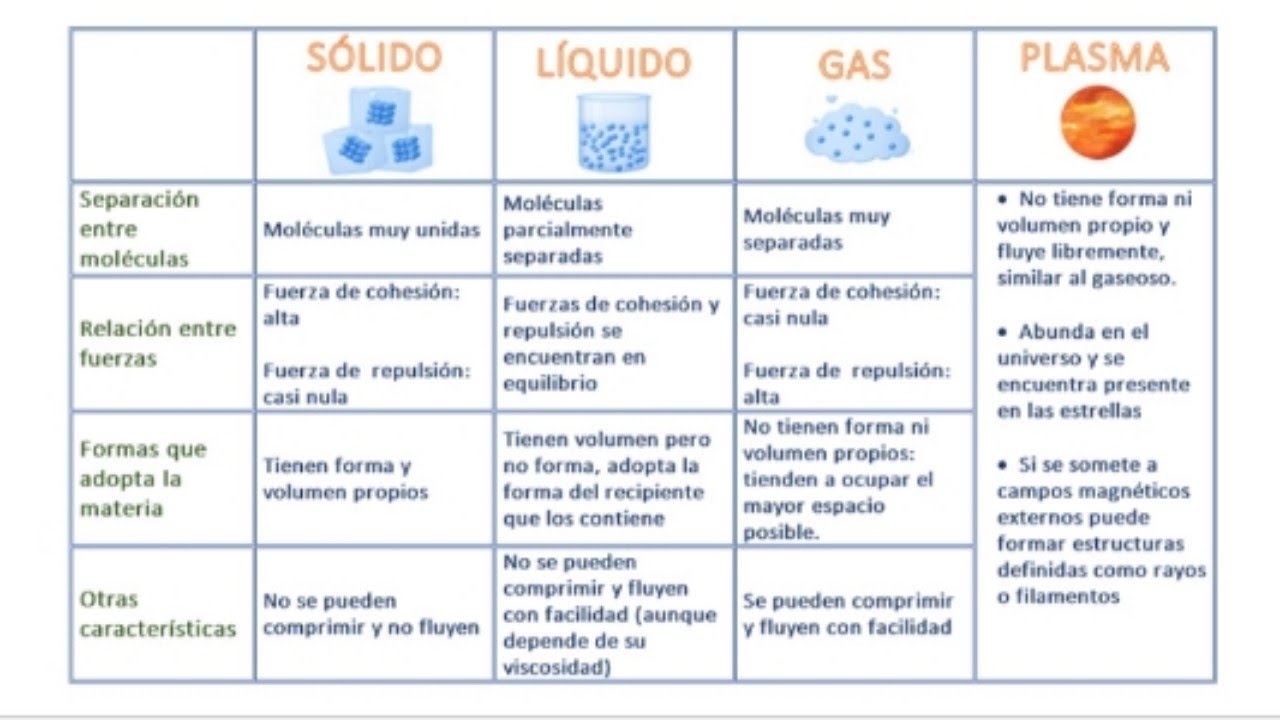
Estado líquido: Algo de movimiento corpuscular pero a baja velocidad (vibración, rotación y traslación corpuscular), fuerzas de atracción medianamente intensas y espacios intercorpusculares algo mayores. Esto hace que los corpúsculos
tengan cierta libertad de movimiento como para deslizarse unos sobre otros y poder fluir. Esto hace que los líquidos puedan adaptarse a la forma del recipiente manteniendo un volumen propio.
Estado gaseoso: Gran libertad de movimiento y a alta velocidad, fuerzas de atracción débil y gran espacio intercorpuscular. Los corpúsculos chocan entre sí y contra las paredes del recipiente generando la presión interna y ocupando todo el volumen disponible. Esto hace que los gases no tengan ni forma ni volumen propio.
Estado sólido: Escaso movimiento (solo vibración corpuscular), baja velocidad,fuerzas de atracción intensas, pequeños espacios intercorpusculares. Los corpúsculos tienen, en general, un ordenamiento particular. Esto hace que los sólidos
tengan forma y volumen propio.
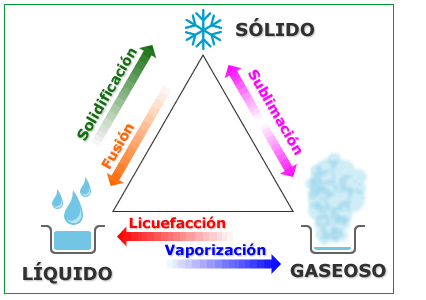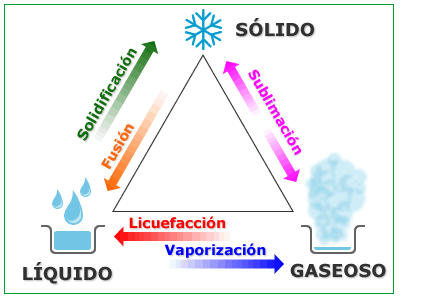
Cambio de estado
Es el proceso por el cual una sustancia pura pasa de un estado de agregación a otro diferente. Los cambios de estado son seis y cada uno de ellos tiene un nombre diferente,
Condensación: Cambio de estado de gas a líquido al disminuir la temperatura
Solidificación: Cambio de estado liquido a solido cuando disminuye temperatura .
https://images.app.goo.gl/FkjBEURd2kYqVD919
Fusión : Cambio de estado de solido a liquido al aumenta su temperatura
Sublimación: Cambio de estado directo solido a vapor al aumentar la temperatura
Vaporización: Cambio de estado de liquido a vapor al aumentar la temperatura
Para cualquier sustancia o mezcla, modificando sus condiciones de temperatura o presión, pueden obtenerse distintos estados o fases, denominados estados de agregación de la materia, en relación con las fuerzas de unión de las partículas (moléculas, átomos o iones) que la constituyen.
https://images.app.goo.gl/hRPVTSGbigqfgJG5A