Antecedentes

https://images.app.goo.gl/46J1aYumqjsATpNV6
Tradicionalmente, la materia se consideraba algo continuo e indivisible hasta que se confirmó que era posible dividirla en partículas más pequeñas, a las que llamamos átomos
El concepto de átomo surgió en Grecia entre un conjunto de filósofos llamados atomistas, entre los que destacan Demócrito y Leucipo.
Aristóteles fue contrario a ellos, defendiendo que la materia era continua. Platón,
aunque proponía la existencia de formas elementales, no creía que éstas fueran indivisibles en otras más pequeñas del mismo tipo.
En la actualidad, el átomo se define como: «La menor partícula constitutiva del elemento que conserva las propiedades de éste y no puede dividirse por métodos químicos», o también como: «La partícula más pequeña de un elemento que puede participar en una combinación química».
Las diferentes teorías que se desarrollaron a lo largo de los años dejaron en claro que esto no era así.
El átomo se compone de un núcleo, el cual es la parte central, allí se encuentran los protones y los neutrones. Es la parte con mayor masa y posee una densidad de 1013 a 1014 g/cm3.
La corona electrónica es la parte exterior del núcleo en donde se encuentran orbitando los electrones alrededor del centro. Ocupan la mayor parte del volumen del átomo. El diámetro de la corona electrónica siempre es superior al núcleo, aunque el núcleo posee mayor masa.
Los electrones y los protones determinan las propiedades químicas de los elementos. Los neutrones no participan en las reacciones químicas en condiciones normales.
En 1808, un científico inglés, el profesor John Dalton, formuló una definición precisa de las unidades indivisibles con las que está formada la materia y que ahora llamamos átomos.
John Dalton es considerado el padre de la teoría atómica debido a que su contribución no fue simplemente proponer una idea original, sino formular claramente una serie de hipótesis sobre la naturaleza de los átomos.
Estas hipótesis señalaban la masa como una de sus propiedades fundamentales y se preocupó por probar tales ideas mediante experimentos cualitativos.
El trabajo de Dalton marcó el principio de la era de la química moderna. Las hipótesis sobre la naturaleza de la materia, en las que se basa la teoría atómica de Dalton, pueden resumirse como sigue:
Los elementos están formados por partículas extremadamente pequeñas llamadas átomos. Todos los átomos de un mismo elemento son idénticos, tienen igual tamaño, masa y propiedades químicas.
Los átomos de un elemento son diferentes a los átomos de todos los demás elementos.
LA ESTRUCTURA DEL ÁTOMO
Con base en la teoría atómica de Dalton, un átomo se define como la unidad básica de un elemento que puede interferir en una combinación química. Una serie de investigaciones iniciadas alrededor de 1850, y que continuaron hasta el siglo XX, demostraron claramente que los átomos tienen una estructura interna, es decir, que están formados por partículas aún más pequeñas, llamadas partículas subatómicas. Estas investigaciones condujeron al descubrimiento de tres partículas: electrones, protones y neutrones.
Descubrimiento de las primeras partículas subatómicas.
Ya a finales del siglo XIX pudieron identificarse, en una serie de experimentos con tubos de descarga de gases, las partículas subatómicas responsables de los fenómenos eléctricos de la materia: en 1886, Goldstein identificó los protones, partículas subatómicas con carga positiva, y en 1897, Thomson identificó los electrones, partículas subatómicas con carga negativa. Además, pudieron determinarse el valor de la masa y de la carga eléctrica de estas partículas subatómicas. A la vista de estos datos podemos destacar dos cosas: 1) la masa de un protón es mucho mayor que la masa de un electrón, casi 2000 veces mayor; y 2) la carga del protón es la misma que la del electrón, pero de signo contrario.
https://images.app.goo.gl/dZpR6yvf4SHn31BS7
Descubrimiento del neutrón.
La masa de protones y electrones por sí sola no coincidía con la masa total del átomo, y Rutherford supuso que en el núcleo tenía que existir otro tipo de partículas subatómicas a las que llamó neutrones, porque creía que no tenían
carga eléctrica. En 1932, J. Chadwick, físico inglés, descubrió estas partículas, que efectivamente no tenían carga eléctrica y cuya masa es ligeramente superior a la del protón. Se encuentran, junto con los protones, en el núcleo de los átomos.
Así, en este nivel, nos quedaremos con el modelo de Bohr incorporando los neutrones en el núcleo. Esto nos permitirá imaginarnos los átomos, representarlos y explicar algunos hechos experimentales y toda una serie de fenómenos que afectan a dichos átomos. 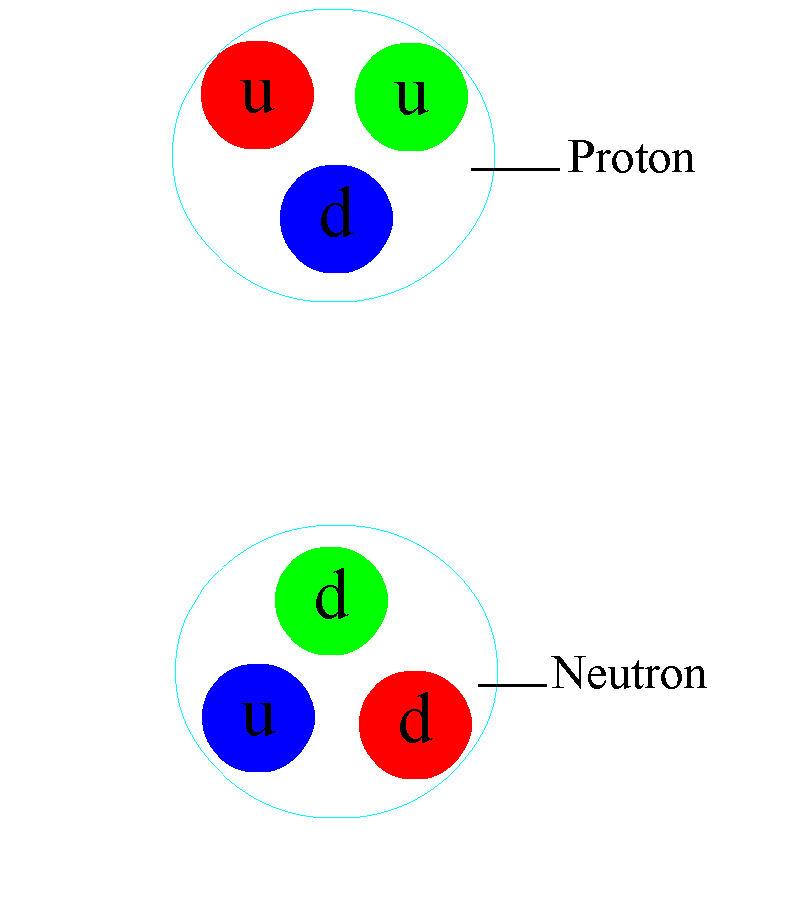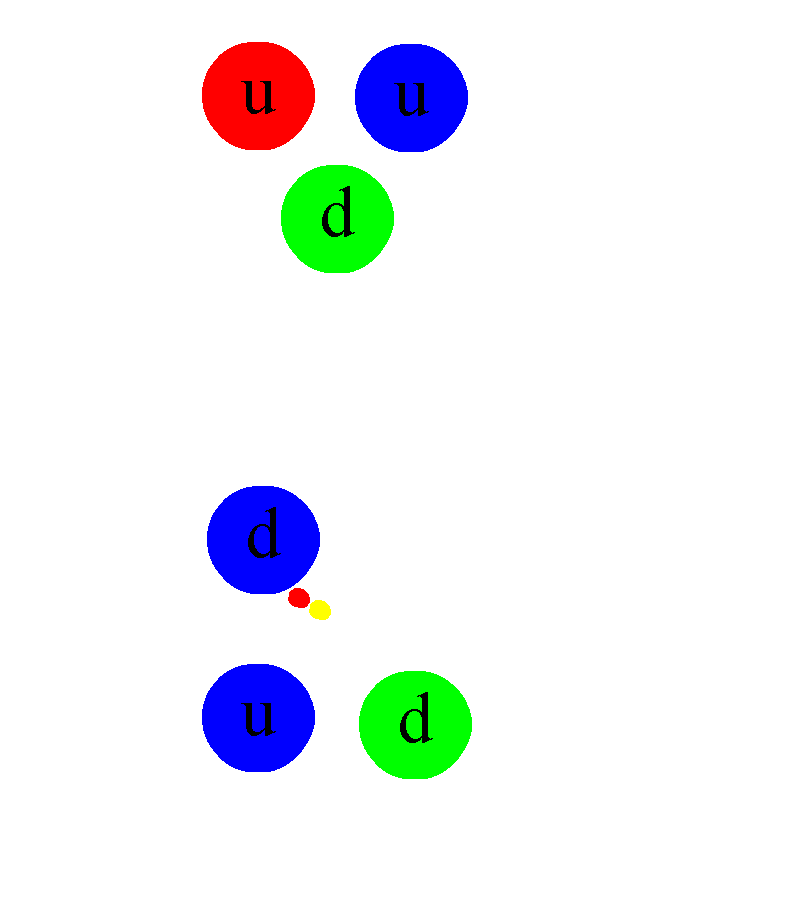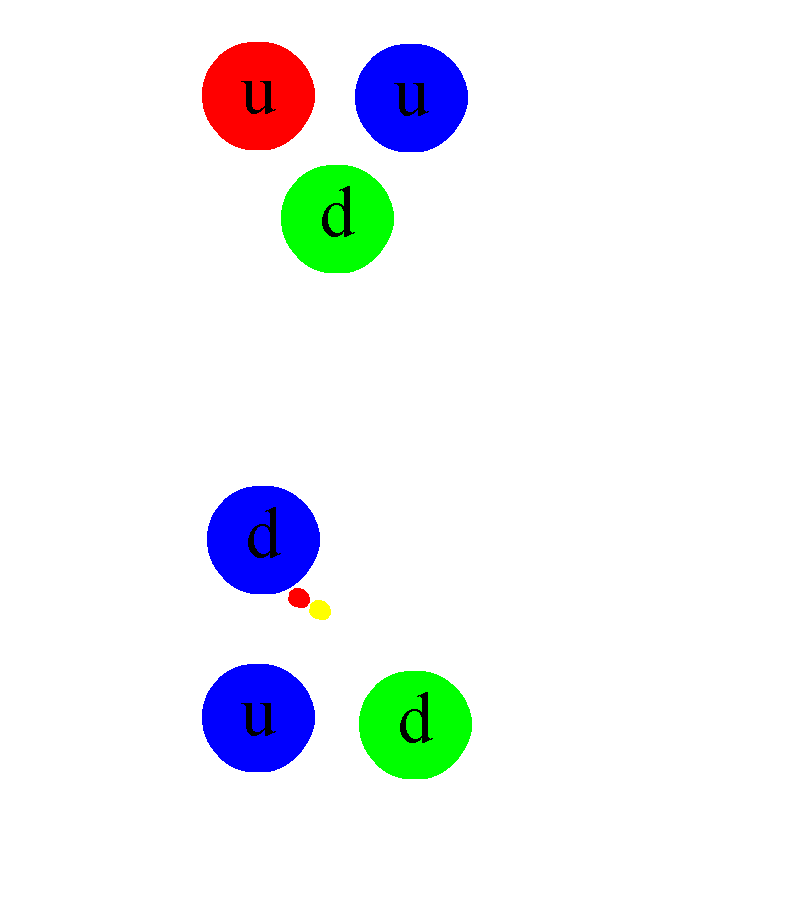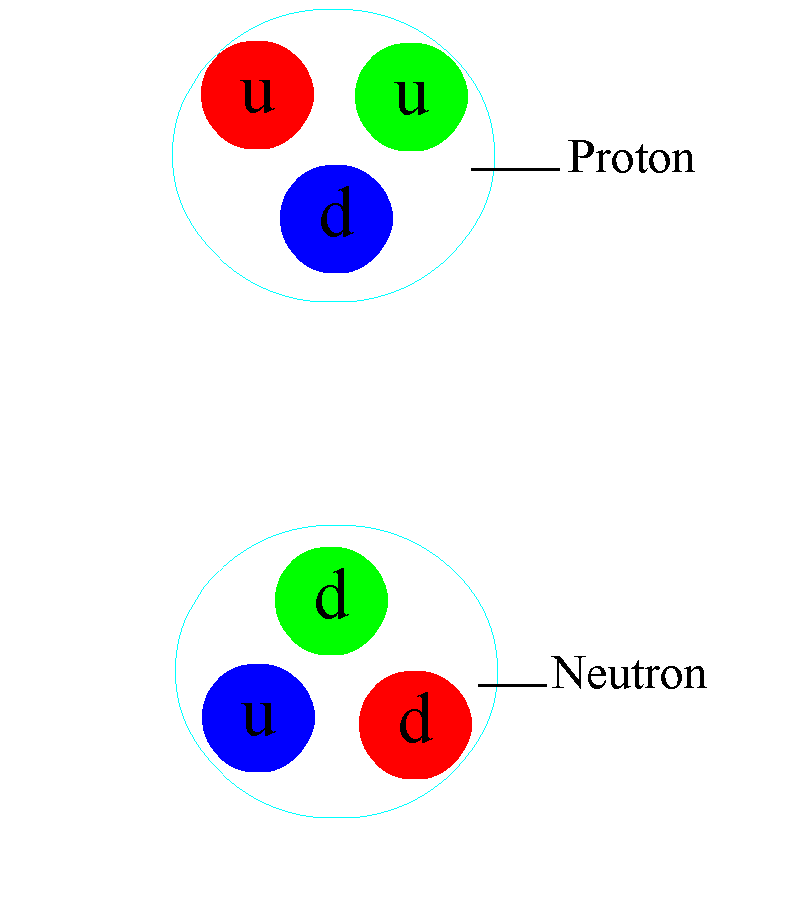
https://images.app.goo.gl/9gJRx6H6mWJmZtZr9
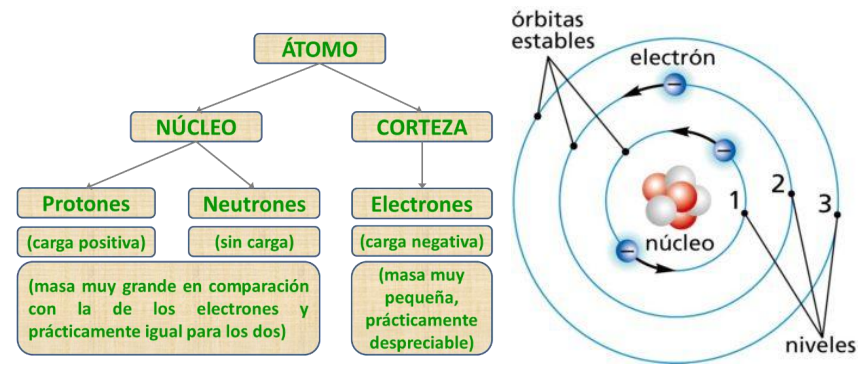
CARACTERIZACIÓN DE LOS ÁTOMOS
Núcleo del átomo
- Dimensiones muy reducidas comparadas con el tamaño del átomo
- En el núcleo radica la masa del átomo
- Partículas: protones y neutrones (nucleones). El número total de nucleones viene dado por el número másico, A.
- Los nucleones están unidos muy fuertemente por la llamada “fuerza nuclear fuerte”
- El número de protones del núcleo es lo que distingue a un elemento de otro.
- El número atómico, Z, nos da el número de protones del átomo y el número de la casilla que éste ocupa en la tabla periódica.
Corteza del átomo
- Los electrones orbitan en torno al núcleo.
- Los electrones (carga -) son atraídos por el núcleo (carga +).
- El número de electrones coincide con el de protones, por eso los átomos, en conjunto, no tienen carga eléctrica
Los átomos de elementos distintos se diferencian en que tiene distinto número de protones en el núcleo (distinto Z).
Los átomos de un mismo elemento no son exactamente iguales, aunque todos poseen el mismo número de protones en el núcleo (igual Z), pueden tener distinto número de neutrones (distinto A).
El número de neutrones de un átomo se calcula así: n = A - Z
Los átomos de un mismo elemento (igual Z) que difieren en el número de neutrones (distinto A), se denominan isótopos.
Todos los isótopos tienen las mismas propiedades químicas, solamente se diferencian en que unos son un poco más pesados que otros. Muchos isótopos pueden desintegrarse espontáneamente emitiendo energía. Son los llamados isótopos radioactivos

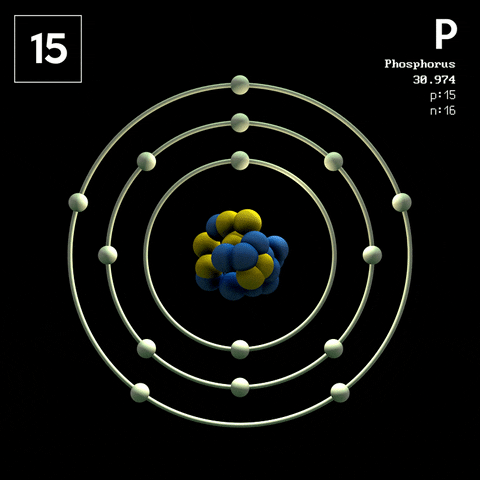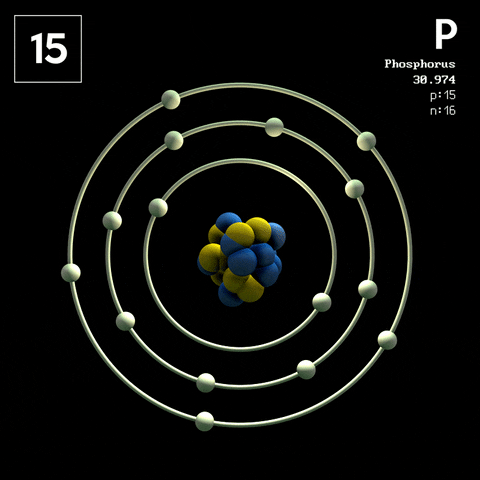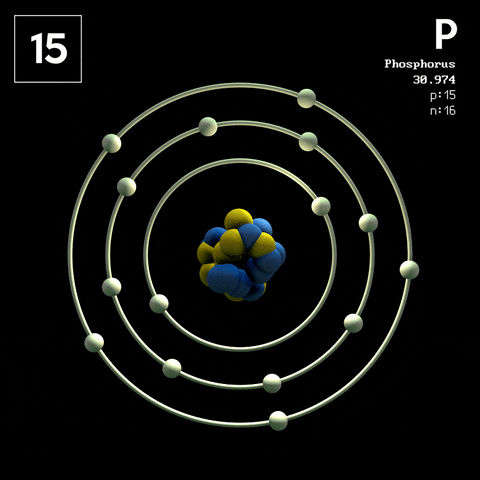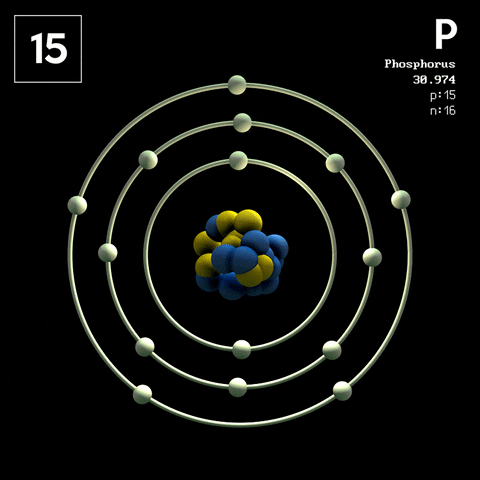
https://images.app.goo.gl/UJnLzwVVx58RoFfx7
Los átomos pueden identificarse gracias al número de protones que contiene su núcleo, ya que este es fijo para los átomos de un mismo elemento. El número de protones de un átomo se llama número atómico y se representa mediante la letra Z, es decir:
NÚMERO ATÓMICO (Z) = NÚMERO DE PROTONES.
Como los electrones apenas tienen masa, la masa de un átomo es prácticamente la suma de las masas de los protones y de los neutrones del núcleo. Por esto, el número de protones y neutrones de un átomo se llama número másico y se representa mediante la letra A, es decir:
NÚMERO MÁSICO (A) = NÚMERO DE PROTONES (Z) + NÚMERO DE NEUTRONES (N)
El número atómico se representa mediante un subíndice situado delante del símbolo del 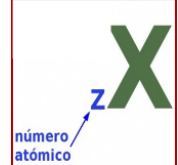
elemento correspondiente y el número másico se representa mediante un superíndice situado delante del símbolo del elemento correspondiente.
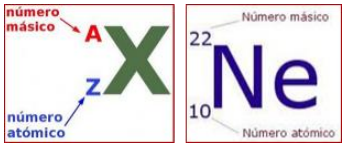
Para identificar un átomo y poder saber cuántas partículas subatómicas (protones, neutrones y electrones contiene, suelen representarse al mismo tiempo, junto con su símbolo, el número atómico(Z) y el número másico (A).
Ten en cuenta lo siguiente: si A = Z + N ![]() N = A – Z. Es decir, conocidos el número atómico (Z) y el número másico (A) de un átomo, podemos calcular fácilmente el número de neutrones (N) que tiene en su núcleo. Así, podemos saber que el átomo de neón representado antes tiene 10 protones y 22 – 10 = 12 neutrones en su núcleo, y 10 electrones en su corteza, ya que es eléctricamente neutro.
N = A – Z. Es decir, conocidos el número atómico (Z) y el número másico (A) de un átomo, podemos calcular fácilmente el número de neutrones (N) que tiene en su núcleo. Así, podemos saber que el átomo de neón representado antes tiene 10 protones y 22 – 10 = 12 neutrones en su núcleo, y 10 electrones en su corteza, ya que es eléctricamente neutro.
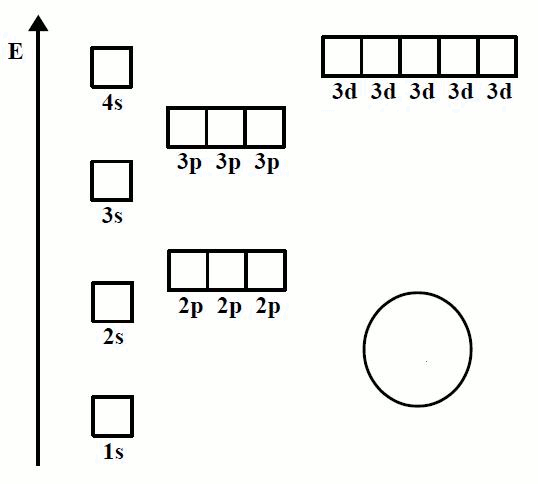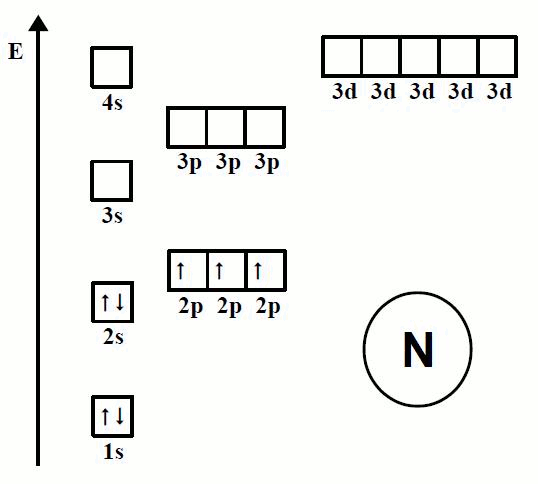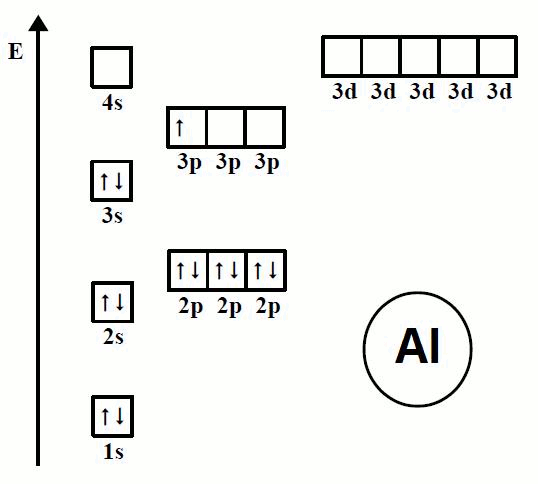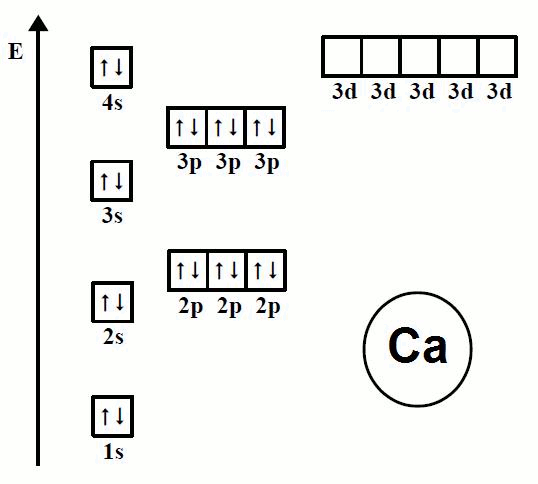
Estructura de la corteza
- Los electrones del átomo se distribuyen en órbitas o capas alrededor del núcleo. En cada capa existen
subcapas o subniveles que se notan por las letras s, p, d y f - Las distintas órbitas se identifican por un número entero, n, llamado número cuántico principal. Así para
la primera capa (la más próxima al núcleo, n = 1; para la segunda n = 2; para la tercera n = 3... - El número de capas u órbitas que posee un elemento viene dado por el número del periodo en que está
situado en la tabla periódica. - La última capa es muy importante desde el punto de vista químico, ya que su estructura va a estar íntimamente relacionada con las propiedades químicas del elemento. Recibe el nombre de capa de valencia.
- Para distribuir los electrones en las capas se deben tener en cuenta unas reglas obtenidas empíricamente 1. Los electrones se distribuyen en las capas ocupando los distintos subniveles que en ellas existen
| CAPA | SUBNIVELES |
| 1 | s |
| 2 | s,p, |
| 3 | s,p,d, |
| 4 | s.p,d,f, |
| 5 | s,p,d,f, |
| 6 | s,p,d,f, |
| 7 | s,p,d,f |
Cada subnivel puede alojar un número máximo de electrones:
| SUBNIVELES | Nº Max |
| S | 2 |
| P | 6 |
| D | 10 |
| F | 14 |